RNNR Rapport du Comité
Si vous avez des questions ou commentaires concernant l'accessibilité à cette publication, veuillez communiquer avec nous à accessible@parl.gc.ca.
|
Après l'arrêt inattendu du réacteur national de recherche universel (réacteur NRU) des laboratoires d'Énergie atomique du Canada limitée (EACL) à Chalk River dans l'Est ontarien le 14 mai 2009, le Comité permanent des ressources naturelles de la Chambre des communes (ci-après le Comité) a tenu plusieurs réunions pour examiner les conséquences de cette interruption au Canada et dans le monde. Après environ 15 mois de travaux de réparation, le réacteur a été remis en service le 17 août 2010. Le présent rapport résume l'étude du Comité et présente des recommandations au gouvernement du Canada sur la production d'isotopes médicaux, l'approvisionnement et la recherche au Canada, notamment sur les mesures de rechange en cette matière. Le réacteur NRU, entré en service en novembre 1957, sert à trois fins :
Le NRU a la capacité d'être le plus important fournisseur mondial d'isotopes médicaux et est l'un des rares réacteurs du monde utilisable pour la recherche et à des fins commerciales. Il accueille chaque année plus de 200 professeurs, étudiants et chercheurs industriels et, selon Dominic Ryan, Ph. D., de l'Institut canadien de la diffusion des neutrons, il est un élément clé des « 50 ans de leadership canadien dans les domaines de la technologie et de la science nucléaires[3] ». Après la fermeture du NRU, les ministres des Ressources naturelles et de la Santé ont créé le Groupe d'experts sur la production d'isotopes médicaux (ci-après le Groupe d'experts) pour examiner les idées et les projets relatifs à leur production. Le Groupe d'experts a présenté son rapport final au gouvernement le 30 novembre 2009. Ce n'est pas la première fois que le réacteur NRU arrête inopinément. En décembre 2007, la Commission canadienne de sûreté nucléaire (CCSN) a arrêté le réacteur à cause d'une contravention aux mesures de sûreté, ce qui a généré des craintes à l'égard d'une éventuelle pénurie mondiale d'isotopes médicaux. Le Parlement du Canada est intervenu en adoptant un projet de loi spécial forçant la remise en service du réacteur NRU. Le tableau 1 présente les coûts d'exploitation et d'immobilisations du réacteur NRU en 2000-2001, en 2004-2005 et en 2008-2009, selon EACL. Tableau 1 - Dépenses d'exploitation et en immobilisations du NRU
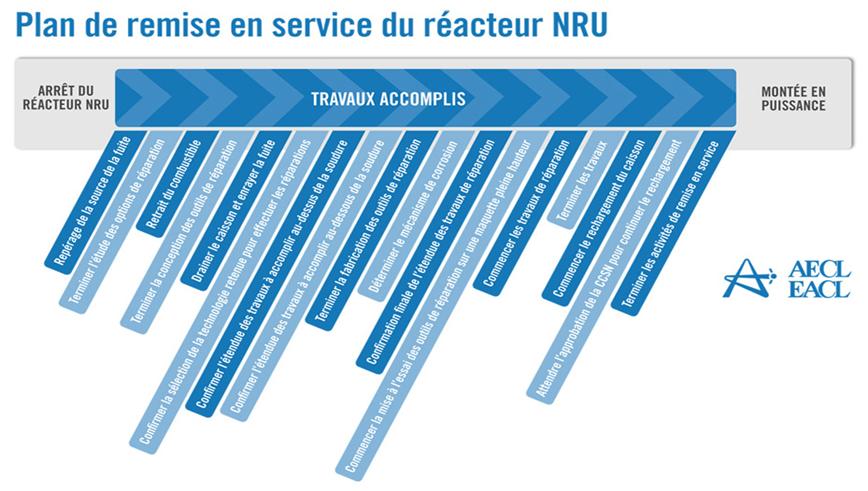
Source : Document présenté au Comité le 20 octobre 2009 par Serge Dupont, conseiller spécial du ministre des Ressources naturelles sur la politique canadienne de l'énergie nucléaire. Avant la fermeture du réacteur NRU, le gouvernement fédéral envisageait de restructurer EACL, et plusieurs enquêtes ont été menées sur l'état général de l'industrie nucléaire. Le présent rapport se concentre sur la panne du NRU et la pénurie consécutive d'isotopes, mais ces considérations plus larges ont une incidence sur la recherche médicale et la production d'isotopes médicaux au Canada. Fondé sur des témoignages variés d'experts canadiens et étrangers, il conclut les audiences du Comité sur le sujet. Le 14 mai 2009, une panne de courant provoque l'arrêt automatique du réacteur NRU. Par la suite, on découvre une fuite d'eau lourde, à un débit de 5 kg/h, et EACL décide de maintenir le réacteur arrêté jusqu'à ce que le problème soit réglé. La fuite résultait de la corrosion de la base de la cuve du réacteur. Dans son témoignage, EACL a indiqué que l'eau lourde écoulée a été recueillie et entreposée dans des fûts et n'a posé aucun risque pour la santé ou la sûreté du public, ni pour l'environnement[4]. Par ailleurs, la quantité de tritium rejetée dans l'atmosphère par évaporation de l'eau lourde était « bien inférieur[e] aux limites réglementaires de la CCSN[5] ». Après des travaux de réparation qui ont duré environ 15 mois, EACL a annoncé, le 17 août 2010, que les tests du NRU étaient terminés et que le réacteur fonctionnait maintenant « à haut régime et [pouvait] commencer à produire des isotopes médicaux ». Les premiers isotopes de molybdène 99 (99Mo) ont été récoltés le 18 août 2010, et le 25 août, EACL a annoncé que le réacteur avait repris « la pleine production d'isotopes médicaux[6]». Pour remettre en service le NRU, EACL a été confrontée à un défi technique sans précédent, étant donné que toutes les activités d'inspection et de réparation de la cuve du réacteur devaient être réalisées à distance, au moyen d'outils spécialisés, par un orifice de 12 cm, à 9 m de la surface corrodée[7]. EACL a donc établi un programme en trois étapes pour le retour en service du NRU :
La figure 1 montre le plan de remise en service du réacteur NRU. Figure 1 : Plan de remise en service du réacteur NRU
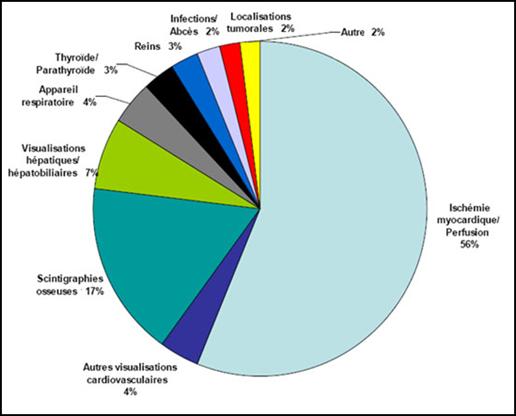
Source : EACL. Selon Hugh MacDiarmid, président-directeur général d'EACL, plusieurs problèmes techniques liés, entre autres, à l'inspection, à l'analyse et à l'interprétation du comportement des métaux irradiés, ainsi qu'à la mesure du stress sur la structure de la cuve[8], ont entravé les progrès des travaux sans précédent de réparation du NRU. Le rechargement du réacteur en combustible nécessitait l'approbation de la CCSN qui, selon William Pilkington, vice-président principal et agent principal du nucléaire d'EACL[9], a été facilitée par le Protocole de redémarrage du réacteur national de recherche universel NRU, établissant le cadre administratif, les jalons et les normes de service pour les activités d'autorisation liées au redémarrage du réacteur NRU[10]. Le réacteur NRU a 52 ans : sa cuve a été remplacée une fois seulement, entre 1972 et 1974, et la cuve actuelle, selon M. Pilkington, a été inspectée plusieurs fois et jugée en bon état pour une longue période encore[11]. Les réacteurs peuvent être remis en état et entretenus sans durée de vie préétablie[12]; cependant, le coût d'entretien et la vulnérabilité croissent avec l'âge[13]. Le 30 mars 2010, M. MacDiarmid a expliqué au Comité que les travaux de réparation restants, devant s'étaler jusqu'à la fin de juillet 2010, coûteraient environ 44 millions de dollars de plus que les 72 millions de dollars attribués par le gouvernement fédéral dans le Budget des dépenses supplémentaires de 2009-2010[14]. Les travaux visent à assurer la fiabilité du fonctionnement du réacteur au-delà de 2016[15]. Le réacteur NRU est autorisé jusqu'en octobre 2011, mais M. MacDiarmid a indiqué que la compagnie cherche avec la CCSN à prolonger la licence jusqu'en 2016[16]. Afin d'être en mesure de bien comprendre les tenants et aboutissants de l'arrêt et de la réparation du réacteur NRU, le Comité s'est rendu à Chalk River le 13 avril 2010. Il a ainsi pu visiter les installations du réacteur NRU et des réacteurs MAPLE (Multipurpose Applied Physics Lattice Experiment). RECOMMANDATION 1 : Compte tenu des témoignages présentés au Comité sur l'arrêt imprévu du réacteur national de recherche universel (NRU), le Comité recommande que le gouvernement fédéral continue d'appuyer le NRU et sa remise en service, et qu'il fournisse tout le soutien nécessaire, d'ordre financier ou autre, pour assurer le renouvellement de sa licence jusqu'en 2016. RECOMMANDATION 2 : Le Comité recommande également que le gouvernement du Canada ordonne à EACL de produire un rapport sur les procédures d'arrêt et de réparation afin de favoriser une meilleure planification et une reprise plus rapide du service advenant un autre arrêt imprévu. CONSÉQUENCES POUR LA MÉDECINE ET LA RECHERCHE DE L'ARRÊT DU RÉACTEUR NATIONAL DE RECHERCHE UNIVERSELA. Conséquences pour la médecineL'arrêt imprévu du réacteur NRU a occasionné une pénurie mondiale d'isotopes médicaux, surtout de molybdène 99 (99Mo), créant ainsi une situation particulièrement problématique pour la médecine. Le technétium 99m (99mTc), produit de désintégration du 99Mo, est utilisé dans près de 82 % des injections de radiopharmaceutiques à des fins diagnostiques, principalement pour l'imagerie cardiaque, les scintigraphies osseuses servant à dépister les cancers et la scintigraphie générale des organes[17]. L'injection de faibles doses de radio-isotopes dans l'organisme génère une énergie qui peut être captée par un dispositif externe pour produire une image diagnostique, ce qui se traduit par un diagnostic plus rapide et plus précis que l'imagerie externe. Dans le cas du cancer, on utilise aussi les radio-isotopes à des fins thérapeutiques en les dirigeant sur des cellules cancéreuses pour que leur énergie les tue[18]. La figure 2 montre la prédominance du 99mTc dans la répartition des procédures de diagnostic en médicine nucléaire au Canada en 2006. Figure 2 - Part des diagnostics
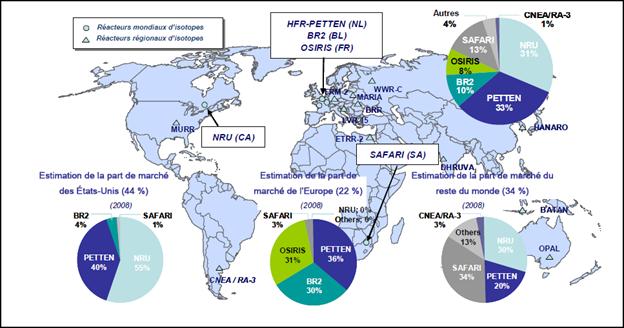
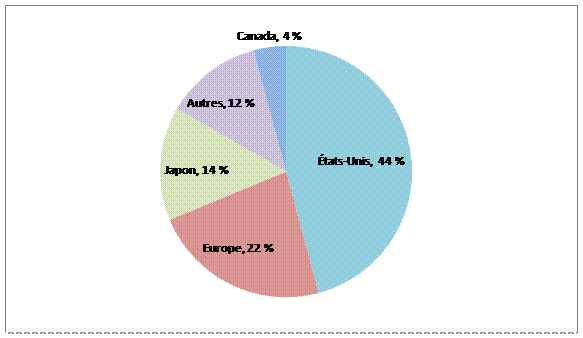
de médecine nucléaire Source : Ressources naturelles Canada. La pénurie d'isotopes a limité le diagnostic, non les traitements. En conséquence, ce sont surtout les patients cancéreux, auxquels il faut un diagnostic précoce et fiable, qui ont été touchés[19]. Suivant l'arrêt du NRU, le Canada a connu une pénurie de 30 %. Elle s'est accentuée à près de 60 % lorsque le réacteur de Petten, aux Pays-Bas, a été fermé temporairement en février 2010[20]. La pénurie a été inégale au Canada, car les approvisionnements sont gérés par les provinces et territoires et parce que la chaîne d'approvisionnement diffère d'une région à l'autre[21]. Selon le Dr Sandy McEwan, conseiller spécial sur les isotopes médicaux pour la ministre de la Santé, Lantheus fournit plus de 99mTc dans l'Est que dans l'Ouest, où Covidien assure la quasi-totalité des approvisionnements[22]. Le Dr McEwan a ajouté que les endroits où on semble avoir eu le plus de difficulté à composer avec la pénurie sont « les petits centres urbains qui dépendent soit des petites radiopharmacies, soit d'un générateur qui est fourni à une radiopharmacie d'hôpital particulière[23] ». La pénurie a aussi entraîné des pertes économiques dans certaines régions. Par exemple, en août 2009, le coût supplémentaire direct des isotopes médicaux pour les hôpitaux et cliniques en Ontario était évalué à environ 1,7 million de dollars[24]. Selon le Dr McEwan, « la situation de nos patients [était] une grande source de préoccupation[25] ». Comme l'a expliqué le Dr Éric Turcotte, du Centre d'imagerie moléculaire de Sherbrooke, la pénurie d'isotopes variait d'une journée à l'autre, ce qui rendait particulièrement difficile de programmer les examens radiopharmaceutiques, même à l'intérieur de 24 heures[26]. Afin de maximiser la quantité de technétium disponible pour les patients, plusieurs départements de médecine nucléaire ont eu recours à des procédures médicales alternatives (parfois moins efficaces) pour composer avec un approvisionnement réduit en 99mTc. Ils ont aussi modifié leurs horaires et dû « établir des priorités, quelquefois reporter des examens et parfois même restreindre le nombre de patients[27] ». Le fait de prioriser les examens selon l'urgence s'est avéré difficile et a pu, dans certains cas, représenter une question de vie ou de mort[28]. B. Offre et demande mondialesCinq réacteurs d'État fournissent environ 95 % de l'approvisionnement mondial en 99Mo : le NRU, le réacteur de Petten, aux Pays-Bas, le réacteur BR2, en Belgique, le réacteur OSIRIS, en France, et le réacteur SAFARI, en Afrique du Sud. Plusieurs autres petits réacteurs fournissent des isotopes pour usage local et régional, sans grand effet sur l'offre mondiale[29]. La figure 3 présente la part mondiale du marché du 99Mo par réacteur en 2008. Figure 3 - Parts du marché mondial du 99Mo en 2008 Source : Réponse du gouvernement du Canada au rapport du Groupe d'experts sur la production d'isotopes médicaux, mars 2010. Selon le groupe interservices ad hoc de la Commission européenne concernant l'approvisionnement en radio-isotopes à usage médical, quelque 30 millions de procédures de diagnostic fondées sur le 99mTc ont été réalisées dans le monde en 2008, dont environ 6 à 7 millions en Europe, 12 à 15 millions en Amérique du Nord, 6 à 8 millions en Asie-Pacifique (notamment au Japon), et 0,5 million dans d'autres régions[30]. Le réacteur NRU permet habituellement de combler de 30 à 40 % de la demande mondiale[31]. Selon EACL, « [l]es isotopes médicaux produits par le NRU aident plus de 76 000 personnes chaque jour et 27 millions de personne chaque année dans plus de 80 pays[32] ». Aux États-Unis, le NRU fournit habituellement environ 50 % des isotopes du marché de ce pays[33]. La figure 4 présente la demande approximative de molybdène 99 et de technétium 99m dans le monde. Figure 4 - Demande mondiale
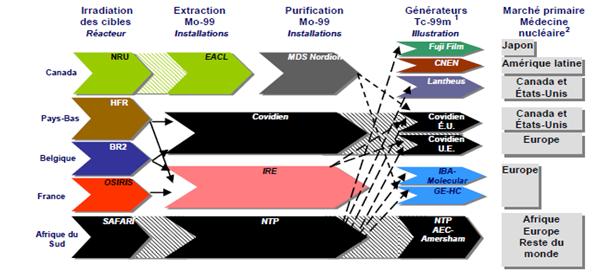
approximative de molybdène 99 Remarque : Le total n'est pas égal à 100 parce que les chiffres ont été arrondis. Source : Ressources naturelles Canada. Il a été d'autant plus difficile de pallier la pénurie mondiale d'isotopes qu'il faut prendre tout au long de la chaîne d'approvisionnement des mesures spécifiques pour satisfaire à diverses exigences techniques et réglementaires. Après avoir été traité au réacteur NRU, le 99Mo, qui a une demi-vie[34] d'environ 66 heures, est expédié à MDS Nordion à Kanata, à quelque 23 km au sud-ouest d'Ottawa, pour être extrait et purifié. Il doit ensuite être exporté à un fabricant de 99mTc aux États-Unis ou au Japon, car il n'en existe pas au Canada. Les exportations aux États-Unis nous reviennent en partie sous forme de générateurs de 99mTc pour nos usages médicaux. Ces générateurs ont une vie utile de 10 à 14 jours et doivent donc parvenir rapidement aux hôpitaux et aux radiopharmacies. Le 99mTc a lui-même une période de seulement six heures, de sorte qu'il est impossible de le stocker. Toutes les étapes de la chaîne d'approvisionnement sont assujetties à des règlements nucléaires et médicaux destinés à assurer la santé et la sécurité[35]. La figure 5 montre la chaîne d'approvisionnement mondial en molybdène 99 et en technétium 99m, ainsi que celle du Canada. Figure 5 - Chaîne
d'approvisionnement mondial Source : Groupe d'experts sur la production d'isotopes médicaux. Comme tous les réacteurs sont mis à l'arrêt à des fins de maintenance systématique, il est essentiel que les fournisseurs d'isotopes harmonisent leurs calendriers afin de maintenir l'équilibre entre l'offre et la demande mondiales[36]. Les représentants des réacteurs du monde se réunissent aux trois mois pour planifier les interruptions et discuter de coordination afin de réduire l'impact des interruptions sur l'offre mondiale[37]. Selon M. Robert Atcher, ex-président de l'International Society of Nuclear Medicine (SNM), le NRU est un réacteur « dont l'excédent de capacité est supérieur à celui des quatre autres réacteurs »; il est ainsi capable de satisfaire « une bonne proportion du marché à approvisionner » quand un des autres grands réacteurs cesse de fonctionner[38]. De plus, la conception du réacteur NRU permet de maximiser la production d'isotopes médicaux puisqu'il a la capacité de continuer la production en période d'entretien planifié et peut être rechargé en cibles et en carburant lorsqu'il est en opération. L'arrêt inattendu et prolongé du NRU a donc causé un grave déséquilibre dans une chaîne d'approvisionnement interdépendante[39]. Selon les prévisions, même si le réacteur NRU était remis en service, il faudra accroître la production d'isotopes médicaux. La demande de technétium 99m, une « technique non invasive » dont les applications ne cessent de croître, est à la hausse partout dans le monde en raison du vieillissement de la population en Europe et en Amérique du Nord et du recours accru aux isotopes dans les pays émergents[40]. Des experts prévoient une demande ferme de technétium 99m pour environ 30 millions d'interventions au cours de la prochaine décennie[41]. Certains témoins ont indiqué que l'interruption du NRU menaçait la viabilité de l'expertise canadienne en médecine nucléaire, ce qui pouvait compromettre le rôle éventuel du pays dans le domaine. Le 19 octobre 2009, le Dr Jean-Luc Urbain, président de l'Association canadienne de médecine nucléaire, a dit au Comité que « le taux d'inscription des étudiants, principalement des technologues et des médecins, dans les sciences de la médecine nucléaire a diminué [.] et les scientifiques de l'énergie nucléaire envisagent de quitter le pays ou l'ont déjà quitté[42] ». Le Dr Kevin Tracey, vice-président de l'Association ontarienne de médecine nucléaire, souligne que la formation des nouveaux techniciens est difficile et « une fois qu'ils quittent la collectivité, [.] ils s'en vont aux États‑Unis. Les convaincre de revenir représente un défi de taille[43] ». RECOMMANDATION 3 : Compte tenu du rôle important que joue le Canada dans la production d'isotopes médicaux, le Comité recommande que le gouvernement du Canada reste en faveur d'une participation canadienne à la production d'isotopes, principalement par l'entremise du Programme de contribution financière à la production d'isotopes ne nécessitant pas de réacteur. RECOMMANDATION 4 : Dans l'intervalle, le Comité recommande que le gouvernement fédéral effectue une analyse coûts-avantages de la production d'isotopes et évalue les niveaux de production d'isotopes dans le futur. RECOMMANDATION 5 : Étant donné la nature intégrée de la chaîne d'approvisionnement d'isotopes internationale, le Comité recommande que le gouvernement fédéral continue de soutenir la coopération et le dialogue avec d'autres fournisseurs d'isotopes à l'échelle internationale, et qu'il continue d'améliorer les protocoles de communication entre les différents intervenants, y compris le public. RECOMMANDATION 6 : Enfin, le Comité recommande que le gouvernement s'efforce de garantir une production soutenue d'isotopes au Canada, de manière à raffermir l'offre de ces produits et à assurer un approvisionnement continu malgré les fluctuations de l'offre à l'échelle internationale. C. Conséquences pour la rechercheOutre la production d'isotopes médicaux, le réacteur NRU sert aussi à la recherche. Selon Dominic Ryan[44], président de l'Institut canadien de la diffusion des neutrons, les faisceaux de neutrons émis par le cour du réacteur permettent d'étudier de nouveaux matériaux, dont « les supraconducteurs haute température critique, grâce auxquels le transport de l'énergie électrique pourrait se faire sans perte, les matériaux de stockage de l'hydrogène, les électrodes de piles permettant une utilisation plus écologique de l'énergie et les composites et superalliages à haute résistance qui révolutionneront la fabrication dans l'avenir ». La recherche et le développement soutiennent l'industrie canadienne en générant des « connaissances uniques [qui] aident les entreprises à concevoir des produits plus compétitifs qui sont sûrs, fiables et de fabrication moins coûteuse ». Le réacteur contribue par ailleurs à « l'intendance [du] parc CANDU [du Canada] et à la conception de la prochaine génération de réacteurs ». Selon M. Ryan, la recherche et la formation soutenues par les installations du NRU « met[tent] le Canada en valeur en tant que chef de file mondiale dans le domaine de la technologie[45] ». Le NRU n'est pas la seule installation de recherche dans le domaine du nucléaire au Canada. Par exemple, le réacteur nucléaire de 5 mégawatts de l'Université McMaster sert principalement à des fins de recherche[46], et les laboratoires de physique subatomique TRIUMF de l'Université de la Colombie-Britannique utilisent la technologie des accélérateurs pour faire de la recherche en physique des particules et en physique nucléaire, y compris l'étude d'isotopes rares[47]. Néanmoins, l'adaptabilité de la conception du NRU crée des possibilités pour la recherche qu'aucune autre installation canadienne ne peut offrir[48]. Les installations utilisant la technologie des accélérateurs ne peuvent remplacer entièrement les réacteurs pour ce qui est de leur rôle dans la recherche nucléaire. Selon Daniel Banks, porte-parole de CREATE (Groupe de travail ad hoc des employés de Chalk River pour un laboratoire national), les installations TRIUMF et de Chalk River sont « complémentaires plutôt que concurrent[e]s » puisque certaines de leurs fonctions de recherche ne sont pas interchangeables. Par exemple, les réacteurs de recherche nucléaire peuvent être utilisés pour « obtenir des connaissances plus précises des conditions, qui ne peuvent être obtenues autrement, des matériaux se trouvant à l'intérieur des réacteurs nucléaires[49]. » Selon M. Banks, « si pour une raison quelconque, nous ne pouvions plus disposer du réacteur NRU et si en même temps, on n'était pas certain de pouvoir exploiter de nouvelles installations, à mon avis, nous assisterions à l'exode d'une masse critique de cerveaux à Chalk River, et probablement très rapidement, tout simplement parce que les scientifiques et les ingénieurs de grand talent qui y travaillent chercheraient alors des emplois ailleurs[50]. » En outre, la fermeture éventuelle du réacteur NRU pourrait provoquer un vide pour bien des scientifiques canadiens et étrangers qui l'utilisent pour la recherche. M. Ryan a expliqué que des équipes d'étudiants des cycles supérieurs et du post-doctorat sont emmenées au réacteur NRU « où une formation pratique leur est offerte par des experts en techniques des faisceaux de neutrons et où ils rencontrent des chercheurs venant de partout sur la planète. C'est la prochaine génération de chercheurs au Canada. Mais si le réacteur n'est pas remplacé, où iront-ils[51]? » Selon Linda Keen, on ignore encore quelle sera l'ampleur du vide qu'entraînerait la fermeture éventuelle du réacteur NRU comme réacteur de recherche[52]. RECOMMANDATION 7 : Compte tenu du rôle essentiel joué par le Canada dans la recherche sur les isotopes médicaux, le Comité recommande que le gouvernement du Canada soutienne la recherche permanente sur les isotopes médicaux. Le Groupe d'experts sur la production d'isotopes médicaux soutient qu'un approvisionnement durable de 99mTc devrait :
En outre, le Groupe d'experts précise que l'approvisionnement sûr de 99mTc devrait :
Les sections qui suivent traitent des principales procédures médicales et options d'approvisionnement citées par les témoins comme moyens actuels ou éventuels de sécuriser et de maintenir les approvisionnements futurs de 99Mo et de 99mTc et d'autres matériaux, et d'éviter que la récente pénurie d'isotopes ne se produise de nouveau. A. Procédures médicales de rechangeLa médecine nucléaire est l'un des nombreux domaines d'application des techniques d'imagerie, et le 99mTc n'est pas le seul isotope à être utilisé pour diagnostiquer le cancer, même s'il sert normalement à environ 82 % des diagnostics par procédure nucléaire. Le tableau 2 compare le 99mTc à une liste d'isotopes médicaux qui pourraient le remplacer à brève échéance, selon le groupe interservices ad hoc de la Commission européenne concernant l'approvisionnement en radio-isotopes à usage médical[54]. En outre, d'autres techniques peuvent remplacer le 99mTc, dont la tomographique par émission de positrons (TEP), la radiographie, la tomodensitométrie (TDM), l'imagerie par résonance magnétique (IRM) et l'échographie[55]. Tableau 2 : 99mTc et isotopes médicaux de rechange
Adapté du rapport du groupe interservices ad hoc de la Commission européenne concernant l'approvisionnement en radio-isotopes à usage medical. Les médecins ont recours à certaines procédures pour pallier les problèmes occasionnés par l'arrêt du NRU, mais celles-ci ne peuvent remplacer le 99mTc que temporairement parce qu'elles sont moins efficaces, accessibles et fiables[56]. L'accès à d'autres procédures, comme la tomodensitométrie et l'IRM, est limité; l'utilisation de l'échocardiographie pour vérifier la fonction cardiaque ne convient pas à 15 ou 20 % des patients[57]; et le thallium génère une dose de radiations beaucoup plus élevée que d'autres radiopharmaceutiques, en plus de produire des images de moins bonne qualité. Si le patient a une légère surcharge pondérale, la qualité de l'image est encore pire, ce qui augmente le risque de poser un diagnostic erroné[58]. De plus, selon le groupe interservices ad hoc de la Commission européenne concernant l'approvisionnement en radio-isotopes à usage médical, aucune alternative n'existe actuellement pour certains composés marqués par du technétium, comme les colloïdes (pour la détection du ganglion sentinelle dans les chirurgies liées au cancer), le MAA pour la scintigraphie pulmonaire de perfusion, le DMSA pour la scintigraphie rénale et le HAS, pour les hémorragies gastro-intestinales et certains examens cardiaques[59]. La pénurie d'isotopes a toutefois eu pour effet d'accroître l'intérêt envers d'autres technologies et des modalités d'imagerie comme la TEP. La TEP ne dépend pas de réacteurs nucléaires parce qu'elle peut utiliser des isotopes fabriqués à partir de cyclotrons installés dans des hôpitaux et des universités. Selon Cyrille Villeneuve, vice-président de Lantheus Imagerie médicale, la technologie constitue une bonne solution de rechange à la technologie conventionnelle offrant « davantage de sensibilité et de précision[60] ». Le Dr Éric Turcotte, professeur et chef clinique du Centre d'imagerie moléculaire de Sherbrooke, s'est dit du même avis, indiquant que la TEP est « de loin le meilleur service que l'on puisse rendre à la population canadienne pour ce qui est du diagnostic du cancer et d'autres problèmes[61]. Bien des experts voient la TEP comme « la technologie de l'avenir[62] ». Par exemple, Nigel Lockyer, directeur de TRIUMF, a mentionné au Comité que l'imagerie TEP est « la composante de la physique nucléaire qui connaît l'essor le plus rapide », ajoutant que « [l]'an dernier, les ventes de caméras TEP aux États-Unis ont été supérieures à celles des caméras TEMP [tomographie d'émission monophotonique] qui utilisent le 99Mo[63] ». Par contre, la technologie est confrontée à plusieurs défis au Canada, dont les suivants :
Selon M. Villeneuve, la technologie de la TEP « devrait prendre davantage d'ampleur dès que l'équipement et l'infrastructure seront bâtis[70] ». M. Meyer a indiqué qu'« au cours des 10 prochaines années, il est assez probable que le Canada opte pour un réseau de production d'isotopes TEP[71] ». Outre la TEP, l'Association canadienne de médecine nucléaire préconise une gamma-caméra utilisant un détecteur à cristal à semi-conducteurs et un logiciel de reprise de résolution. Selon le Dr Urbain, la nouvelle caméra est « la solution [à court, moyen et long termes] applicable immédiatement » qui utilise de deux à trois fois moins de 99mTc que les appareils de TEM conventionnels[72]. RECOMMANDATION 8 : Compte tenu de ce témoignage, le Comité recommande que le gouvernement fédéral favorise au besoin le recours à d'autres isotopes médicaux pour les diagnostics. RECOMMANDATION 9 : De plus, le Comité recommande que le gouvernement du Canada encourage le développement de la technologie d'émission de positrons à la lumière des essais précliniques et cliniques effectués en Europe et aux États-Unis. B. Options d'approvisionnement du CanadaConformément aux efforts déployés à l'échelle internationale à l'égard de la non-prolifération nucléaire, l'utilisation d'uranium faiblement enrichi (UFE) dans les réacteurs nucléaires à des fins civiles commence à prendre le pas sur l'uranium hautement enrichi (UHE). L'UFE a une concentration d'U‑235 inférieure à 20 %, alors qu'elle est de 93 % dans l'UHE. Ce dernier, qui sert également à la production d'armes nucléaires, a été l'option privilégiée pour la production d'isotopes parce que hausser la concentration d'U-235 à plus de 90 % permet de maximiser la production de 99Mo. La production à grande échelle de 99Mo à partir de cibles d'UFE doit encore faire l'objet de recherche-développement, d'une part pour optimiser le processus de production d'isotopes et d'autre part, pour gérer la hausse du volume de déchets[73]. Les sections qui suivent traitent des principales options technologiques pour la production d'isotopes médicaux au Canada selon le Groupe d'experts et différents témoins. Le tableau 3 résume les renseignements disponibles sur chacune des options. Pour une foule de raisons, le Comité n'a pas obtenu l'information nécessaire pour réaliser une analyse coûts-avantages des coûts en capital ou de production définitifs de chaque option. Tableau 3 : Renseignements clés sur les options technologiques proposées
* La capacité de produire du 99Mo au moyen d'un réacteur utilisant des cibles d'UFE est limitée davantage par l'efficience de l'installation de production que par le réacteur comme tel. ** D'après l'estimation de la demande canadienne de 99mTc, qui se chifrre à 32 000 doses (470 Ci de six jours de 99Mo brut) par semaine. *** D'après la capacité estimée du réacteur, sans égard aux limites de l'installation de production. Adapté du Rapport du Groupe d'experts sur la production d'isotopes médicaux. Nouveau réacteur de recherche polyvalentLe Groupe d'experts soutient que la construction d'un nouveau réacteur de recherche polyvalent est l'option qui présente « le plus grand nombre d'avantages concomitants, compte tenu de l'importance des recherches prévues et de leurs retombées en matière de propriété intellectuelle, de création d'emplois et de formation ». De plus, comme le NRU approche la fin de sa vie utile, « il est important de prendre rapidement une décision [.] afin de minimiser tout écart entre le démarrage de ce nouveau réacteur et la fermeture permanente du réacteur NRU[74] ». Le Groupe d'experts reconnaît qu'il s'agit de l'option la plus coûteuse et souligne que même si les coûts de la construction d'un nouveau réacteur peuvent être partagés entre plusieurs activités, la production des isotopes ne compense que de 10 à 15 % de ces coûts. Il conclut donc que la construction d'un nouveau réacteur doit être justifiée, dans une large mesure, grâce aux autres missions qu'on pourrait lui confier. Il a par ailleurs recommandé que tout nouveau réacteur produisant du 99Mo devra utiliser des cibles d'uranium faiblement enrichi, conformément aux efforts internationaux en matière de non-prolifération nucléaire. Si l'on utilise de l'uranium faiblement enrichi, il sera nécessaire de procéder à des activités de recherche-développement pour optimiser la production d'isotopes et gérer les importants volumes de déchets[75]. Le Centre canadien des neutrons, à Chalk River, a été proposé pour remplacer le réacteur NRU en tant que nouveau réacteur de recherche polyvalent capable de produire du 99Mo dès sa conception. En outre, selon M. Serge Dupont, « La province de la Saskatchewan s'est également dite intéressée à discuter avec le gouvernement du Canada pour peut-être conclure des arrangements concernant un réacteur de recherche et, éventuellement, la production d'isotopes[76]. » RECOMMANDATION 10 : Le Comité recommande que le gouvernement du Canada étudie la faisabilité d'un nouveau réacteur de recherche multifonction afin d'évaluer avec précision les coûts de construction et d'exploitation, ainsi que les sources de revenus possibles, et qu'il présente les résultats de son étude au Parlement. Réacteurs MAPLELes réacteurs MAPLE (Multipurpose Applied Physics Lattice Experiment) 1 et 2, situés aux laboratoires d'EACL à Chalk River, ont été conçus et construits exclusivement pour produire, à contrat, des isotopes médicaux. Initialement destinés à remplacer la production d'isotopes du réacteur NRU vieillissant, ils n'ont jamais été pleinement mis en service parce que leur comportement n'était pas conforme à celui de la modélisation. Selon EACL, ils ne satisfaisaient pas aux exigences de sécurité, car l'écart ne s'expliquait pas clairement. M. MacDiarmid a déclaré au Comité que les réacteurs MAPLE ont coûté à EACL 250 millions de dollars[77], ce qui exclut la part assumée par MDS Nordion. Les réacteurs sont présentement en mode d'arrêt prolongé[78]. Les avis sont partagés sur la possibilité de relancer le projet des réacteurs MAPLE. Jatin Nathwani, titulaire d'une chaire de recherche de l'Ontario en politiques publiques et en gestion de l'énergie renouvelable, Jean Koclas, professeur à l'Institut de génie nucléaire de l'École polytechnique Montréal, et Daniel Meneley, doyen par intérim de la Faculty of Energy Systems and Nuclear Science de l'University of Ontario Institute of Technology, se sont exprimés en faveur de la relance du projet, M. Meneley déclarant que « en dépit des faiblesses évidentes associées aux réacteurs MAPLE, [.] le redémarrage et la mise en service de ces installations sont sans doute la voie à privilégier[79] ». En outre, Steve West, président de MDS Nordion, a cité un rapport de la National Academy of Sciences qui affirme qu'EACL pourrait probablement conclure un contrat avec un autre organisme afin de se procurer l'expertise ou les ressources techniques nécessaires pour corriger les réacteurs MAPLE. Le comité qui a rédigé le rapport « suppose que le pire des scénarios pour corriger les réacteurs MAPLE comporte le remplacement des cours des réacteurs », ce qui coûterait probablement moins cher que d'en construire un nouveau[80]. Par contre, John Waddington, consultant en sûreté nucléaire, a indiqué que les réacteurs pourraient en principe être mis en service, mais a ajouté que cela nécessiterait « beaucoup [.] d'efforts humain[s] et financier[s][81] ». Par ailleurs, Hugh MacDiarmid, estime que les réacteurs MAPLE ne sont pas une option viable à court terme puisqu'il faudrait « bien des années et des centaines de millions de dollars avant qu'ils reçoivent une licence et soient mis en service[82] ». Le Groupe d'experts soutient que les réacteurs MAPLE, qui sont conçus exclusivement pour la production d'isotopes à partir d'UHE, « engendre[nt] d'importants défis en ce qui a trait à d'éventuelles adaptations [.], pour la planification d'une conversion à l'UFE ». En outre, le Groupe d'experts a indiqué que « même si les infrastructures existantes ne coûtaient rien, la rationalité économique d'un [.] projet [MAPLE] soulève des interrogations en raison des coûts d'opération élevés impossibles à répartir entre plusieurs fonctions[83] ». Les réacteurs MAPLE ne pourraient générer tous les isotopes produits par le réacteur NRU, dont le cobalt-60 (utilisé pour le traitement du cancer) et d'autres isotopes à des fins industrielles, et servir à la recherche sur les matériaux avancés[84]. Recommandation 11 : Si le secteur privé présente pour les réacteurs MAPLE une proposition qui tient pleinement compte des risques commerciaux associés aux réacteurs et qui ne nécessite pas l'engagement de coûts supplémentaires de la part du gouvernement, le Comité recommande que le gouvernement du Canada demeure disposé à examiner la proposition. Réacteur nucléaire de McMasterLe réacteur nucléaire de l'Université McMaster de Hamilton, en Ontario, est un réacteur d'essais de matériaux (materials test reactor - MTR) de 5 mégawatts. L'Université a proposé de produire assez de 99Mo pour satisfaire à environ 20 % de la demande nord-américaine à moyen terme, soit près de quatre fois la demande canadienne[85]. Le réacteur a déjà produit des isotopes médicaux dans les années 1970. Toutefois, la chaîne d'approvisionnement actuelle n'est pas conçue pour intégrer de grandes quantités d'isotopes produites à Hamilton (Ontario). De plus, M. Christopher Heysel, directeur Activités et installations nucléaires, réacteur nucléaire McMaster, a indiqué que même si la production d'isotopes proposée aura la même composition chimique pour les cibles, la cible du réacteur NRU comporte une géométrie différente de celle du réacteur McMaster, qui se présente sous forme plissée[86]. EACL a fait savoir qu'elle était favorable à la proposition de McMaster « sous toute réserve », soulignant que des problèmes d'ordre logistique liés au transport de matières radioactives dans les régions du Grand Toronto et de Hamilton pourraient entraver la mise en ouvre de cette option[87]. Le Groupe d'experts a fait valoir que le recours à d'autres réacteurs de recherche ou de puissance existants pour l'irradiation de cibles destinées à la production de 99Mo exige l'utilisation de cibles d'UHE pour obtenir une production rentable et que, conformément aux efforts internationaux en matière de non-prolifération nucléaire, les options fondées sur l'utilisation de l'UHE devraient être considérées comme alternative pour répondre aux pénuries à court terme. Convertir un réacteur pour passer des cibles d'UHE (à environ 93 % de U-235) à des cibles UFE (moins de 20 % de U-235) conduit à une baisse de la production d'isotopes à un cinquième de son efficience pour une même quantité d'uranium et nécessite des modifications structurelles (conception de nouvelles cibles). Cela entraîne par ailleurs d'autres coûts en raison des rendements faibles et de l'augmentation des déchets[88]. Selon le site Web de l'Université McMaster, « le réacteur [McMaster] subit actuellement une conversion de l'uranium hautement enrichi à l'uranium faiblement enrichi [.][89] ». Le réacteur McMaster, dont le permis d'exploitation expirera en 2014, fonctionne à 3 mégawatts, 16 heures par jour, cinq jours par semaine. Selon McMaster, il devrait fonctionner 24 heures sur 24, 7 jours sur 7 pour produire la quantité d'isotopes proposée. CyclotronsLes cyclotrons sont des accélérateurs de particules circulaires. Même s'ils produisent déjà certains isotopes médicaux (comme le thallium 201, l'iode 125 et le gallium 67), ils ne peuvent encore produire de 99mTc pour usage médical à grande échelle. Selon Tim Meyer, les cyclotrons actuels ont la capacité de produire des quantités limitées de 99mTc en bombardant du molybdène 100 avec des protons. Des essais cliniques chez les humains pourraient être réalisés dans un délai de 18 mois, et la technologie pourrait être déployée sans qu'il ne soit nécessaire d'apporter d'importantes modifications au matériel déjà en service au Canada. Par contre, les isotopes produits par des cyclotrons ont une courte demi-vie, ce qui limite leur utilisation aux hôpitaux et radiopharmacies locaux. Selon M. Meyer, cela ne semble toutefois pas être un gros problème étant donné que la plupart des régions habitées du Canada sont concentrées près des grands centres démographiques[90]. Le Comité se préoccupe du fait que si les cyclotrons n'étaient installés qu'à proximité des grands centres démographiques, certaines communautés rurales pourraient y avoir accès plus difficilement. Selon le Groupe d'experts, il est difficile d'évaluer la part du marché canadien susceptible d'être couverte par les cyclotrons étant donné que cette technologie est encore au stade de développement. Toutefois, cette option est intéressante car l'infrastructure des cyclotrons peut être utilisée pour d'autres fins tout en constituant une source d'approvisionnement supplémentaire[91]. Le Comité ignore combien coûtera l'option des cyclotrons. Selon le Groupe d'experts, les coûts des activités intensives de recherche-développement pour la production de 99mTc à partir de cyclotrons peuvent être relativement faibles étant donné qu'on dispose déjà de l'infrastructure nécessaire pour entreprendre la recherche, la démonstration et la production initiale. Toutefois, la production et la commercialisation à grande échelle du 99mTc pourraient être très coûteuses en raison de la rareté du 100Mo, qui n'est pas produit commercialement[92]. La production de 99mTc à partir de cyclotrons pourrait demander une validation plus approfondie par les organismes de réglementation en matière de santé, par rapport à d'autres options. Par contre, les cyclotrons ne produisent pas de déchet nucléaire et constituent une option avantageuse en matière de calendrier. Selon les résultats de la recherche-développement et les questions de réglementation, la production commerciale du 99mTc pourrait commencer entre 2011 et 2014[93]. Accélérateurs linéairesOption de la photofissionLe groupe TRIUMF de l'Université de la Colombie-Britannique (UBC) a proposé une autre méthode de production de 99Mo grâce aux interactions nucléaires avec l'uranium naturel. Dans l'option de la photofission, « un accélérateur linéaire d'électrons de haute énergie bombarderait un convertisseur pour créer un faisceau intense de photons afin de produire du 99Mo grâce aux interactions nucléaires avec l'uranium naturel[94] ». Un nouveau réacteur de recherche polyvalent, le e-linac ou accélérateur d'électron linéaire supraconducteur, est en voie de construction à l'UBC et servira à valider cette option[95]. Selon le Groupe d'experts, le concept de la photofission nécessite d'importantes activités de recherche-développement pour la conception de la cible et du convertisseur, la capacité de refroidissement et l'optimisation de l'ensemble du processus. Cette technologie s'intégrerait facilement dans la chaîne d'approvisionnement, mais elle générerait d'importantes quantités de déchets nucléaires. En outre, pour atteindre les niveaux de production requis, l'accélérateur doit être uniquement dédié à la production d'isotopes, ce qui est loin d'être rentable puisque l'important investissement en immobilisations ne peut être réparti en plusieurs missions[96]. Option de la transmutation du 100MoUn accélérateur linéaire d'électrons peut produire du 99Mo par la transmutation de 100Mo, une option proposée par le Conseil national de recherche[97]. Selon le Groupe d'experts, « cette option exige d'importantes activités de R. et D. en ce qui concerne la conception des cibles et les capacités de refroidissement, de même que la mise au point et la commercialisation d'un nouveau type de générateur ». Des doutes ont également été émis selon lesquels les hôpitaux pourraient refuser l'utilisation des nouveaux générateurs et que ce produit ne soit donc pas en mesure de concurrencer les générateurs classiques[98]. Selon le Groupe d'experts, le 100Mo purifié n'est actuellement pas produit commercialement. Le coût de production des quantités nécessaires risque d'être élevé, faisant ainsi obstacle à la mise en marché. On ignore si un recyclage complet du 100Mo pourrait réduire substantiellement les coûts, car la possibilité d'un tel recyclage reste à démontrer, ce qui exigera des efforts importants en matière de recherche-développement. En outre, pour produire les quantités voulues, ce type d'accélérateur devrait probablement servir uniquement à la production d'isotopes, ce qui, à l'instar de la photofission, amoindrit la rentabilité de cette option. Du point de vue environnemental, le Groupe d'experts a indiqué que cette option est plus avantageuse que l'option de la photofission parce qu'elle ne génère aucun déchet nucléaire[99]. RECOMMANDATION 12 : Le Comité recommande que le gouvernement fédéral tire leçon de l'échec des réacteurs MAPLE et de l'incidence qu'a eu la fermeture du NRU sur l'approvisionnement au Canada, et qu'il cherche à diversifier et à sécuriser ses sources d'approvisionnement en isotopes médicaux à moyen et à long termes, en finançant plusieurs projets à même l'enveloppe de 35 millions de dollars annoncés dans le dernier budget fédéral. RECOMMANDATION 13 : Le Comité recommande en outre que le gouvernement fédéral étudie à fond tous les projets de production de produits de remplacement et continue de soutenir la recherche et le développement de nouvelles technologies. RECOMMANDATION 14 : En particulier, le Comité recommande que le gouvernement continue de financer la recherche dans le domaine de la technologie des accélérateurs, tant les accélérateurs linéaires que les cyclotrons. C. Fournisseurs hors du CanadaPeu après l'arrêt du réacteur NRU, le réacteur de Petten aux Pays-Bas a accru sa production de 50 % et le réacteur SAFARI en Afrique du Sud, de 20 %. En outre, la Belgique a accru sa capacité de traitement « en raison des plus grands volumes d'irradiation par les réacteurs européens » et l'Australie a « intensifié ses efforts pour remettre son réacteur OPAL en service[100] ». L'Australie a également commencé à produire des isotopes médicaux pour ses besoins intérieurs, ce qui libère l'offre de l'Afrique du Sud pour l'exportation vers un autre pays[101]. La situation a toutefois changé lorsque le réacteur de Petten a été interrompu temporairement comme prévu, en février 2010, ce qui a aggravé considérablement la pénurie mondiale. Malgré d'importants efforts déployés à l'échelle internationale pour produire des isotopes supplémentaires, l'offre mondiale d'isotopes médicaux demeure, au mieux, instable. Tous les grands réacteurs qui en produisent ont à peu près l'âge du NRU (voir le tableau 2) et la viabilité de leur production d'isotopes est incertaine. En outre, ils doivent tous subir des arrêts prévus de maintenance[102]. Tableau 4 - Âge des grands réacteurs de production
Source : Ressources naturelles Canada. D'autres réacteurs pourraient contribuer éventuellement à l'offre mondiale d'isotopes médicaux. Mentionnons un réacteur argentin, qui pourrait exporter de modestes quantités en Amérique du Nord; le réacteur Jules Horowitz en France, qui doit entrer en service d'ici 2015; enfin, le réacteur de recherche de l'Université du Missouri qui pourrait être adapté pour produire du 99Mo, malgré qu'il n'y ait encore rien d'engagé pour cela[103]. RECOMMANDATION 15 : Le Comité recommande que le gouvernement reconnaisse que le réacteur NRU, étant donné son âge, ne constitue pas une solution à long terme crédible ou durable, mais qu'il demeure d'une importance critique pour l'approvisionnement à court terme en isotopes, tant à l'échelle nationale qu'à l'échelle internationale. Le gouvernement du Canada a fait savoir qu'il a pris des mesures en réponse à l'arrêt du réacteur NRU et à la pénurie consécutive d'isotopes médicaux, à savoir :
Le budget de 2010 prévoit par ailleurs une somme de 300 millions de dollars (comptabilité de caisse) en 2010-2011 pour couvrir « des pertes commerciales anticipées et appuyer les activités d'EACL, notamment la poursuite des travaux d'élaboration du réacteur CANDU avancé, la fourniture sécuritaire d'isotopes médicaux et le maintien d'activités fiables et sécuritaires aux laboratoires de Chalk River[106] ». Selon Hugh MacDiarmid, ces fonds serviront à appuyer un certain nombre d'activités, « dont quelques-unes sont liées à la réparation du réacteur NRU et aux préparatifs pour présenter une nouvelle demande de permis ou la prolongation du permis du réacteur NRU[107] ». RECOMMANDATION 16 : Outre ces mesures, le Comité recommande que le gouvernement du Canada veille à dédommager les provinces et les territoires pour l'augmentation du coût du technétium 99m et les coûts de gestion supplémentaires auxquels ont dû faire face les autorités de la santé à la suite de la pénurie d'isotopes médicaux. RECOMMANDATION 17 : Le Comité recommande également que le gouvernement fasse une déclaration publique afin d'indiquer clairement s'il a l'intention de se retirer du volet offre de la production d'isotopes d'ici 2016. RECOMMANDATION 18 : Si le gouvernement a l'intention de se retirer du secteur de la production d'isotopes, comme l'a indiqué le premier ministre, le Comité recommande qu'il fasse une déclaration publique et dépose une stratégie de retrait détaillée, y compris ses plans concernant le maintien en service du réacteur NRU jusqu'en 2016. [1] Le réacteur CANDU est un réacteur de puissance conçu au Canada qui utilise l'uranium naturel comme combustible et l'eau lourde comme modérateur et caloporteur. [2] EACL, « Sciences nucléaires - Profil du réacteur National Research Universal », sans date, http://www.eacl-aecl.ca/Sciences/CRL-f/NRU-f.htm. [3] Dominic Ryan, Institut canadien de la diffusion des neutrons, Témoignages, 16 juin 2009. [4] William Pilkington, EACL, Témoignages, 4 juin 2009. [5] Michael Binder, CCSN, Témoignages, 4 juin 2009. [6] Bulletins de renseignements de Chalk River, EACL, http://www.eacl-aecl.ca/NewsRoom-f/Newsletters.htm. [7] William Pilkington, EACL, Témoignages, 19 octobre 2009. [8] Hugh MacDiarmid, EACL, Témoignages, 30 mars 2010. [9] William Pilkington, EACL, Témoignages, 19 octobre 2009. [10] « EACL et la CCSN signent un protocole », EACL, http://www.nrucanada.ca/fr/accueil/projectrestart/aeclcnscprotocol.aspx. [11] William Pilkington, EACL, Témoignages, 21 août 2009. [12] Michael Binder, CCSN, Témoignages, 4 juin 2009. [13] Serge Dupont, Ressources naturelles Canada, Témoignages, 2 juin 2009. [14] Hugh MacDiarmid, EACL, Témoignages, 30 mars 2010. [15] William Pilkington, EACL, Témoignages, 19 octobre 2009. [16] Hugh MacDiarmid, EACL, Témoignages, 4 juin 2009. [17] Meena Ballantyne, Direction générale des produits de santé et des aliments, Santé Canada, Témoignages, 2 juin 2009, et Cyrille Villeneuve, Lantheus Imagerie Médicale, Témoignages, 25 mars 2010. [18] Medical Isotopes, Frequently Asked Questions, 12 mars 2008, http://www.medicalisotopes.org/faq.html. [19] Karen Gulenchyn, Département de médecine nucléaire, Hamilton Health Sciences et St. Joseph's Healthcare Hamilton, Témoignages, 9 juin 2009. [20] Éric Turcotte, Centre d'imagerie moléculaire de Sherbrooke, à titre personnel, Témoignages, 25 mars 2010. [21] Jean-Luc Urbain, Association canadienne de médecine nucléaire, Témoignages, 9 juin 2009. [22] Sandy McEwan, conseiller spécial sur les isotopes médicaux pour la ministre de la Santé, à titre personnel, Témoignages, 19 août 2009. [23] Ibid., 21 août 2009. [24] David Caplan, ministre de la Santé et des Soins à long terme, gouvernement de l'Ontario, Témoignages, 21 août 2009. [25] Sandy McEwan, conseiller spécial sur les isotopes médicaux pour la ministre de la Santé, à titre personnel, Témoignages, 21 août 2009. [26] Éric Turcotte, Centre d'imagerie moléculaire de Sherbrooke, à titre personnel, Témoignages, 25 mars 2010. [27] Cyrille Villeneuve, Lantheus Imagerie Médicale, Témoignages, 25 mars 2010. [28] Éric Turcotte, Centre d'imagerie moléculaire de Sherbrooke, à titre personnel, Témoignages, 25 mars 2010. [29] Serge Dupont, Ressources naturelles Canada, Témoignages, 2 juin 2009. [30] Groupe ad hoc interservices de la Commission européenne concernant l'approvisionnement en radio-isotopes à usage médical, Preliminary Report on Supply of Radioisotopes for Medical Use and Current Development in Nuclear Medicine, 30 octobre 2009. [31] Serge Dupont, Ressources naturelles Canada, Témoignages, 2 juin 2009. [32] EACL, « Sciences nucléaires - Isotopes médicaux », sans date, http://www.eacl-aecl.ca/Sciences/CRL-f/NRU-f/Isotopes-f.htm. [33] Robert Atcher, International Society of Nuclear Medicine, Témoignages, 21 août 2009. [34] La « demi-vie » d'un isotope est le temps requis pour qu'une quantité donnée de matériel radioactif diminue de moitié en raison de la désintégration. Par exemple, le 99mTc, dont la demi-vie est de six heures, perd la moitié de sa radioactivité toutes les six heures. [35] Serge Dupont, Ressources naturelles Canada, Témoignages, 2 juin 2009. [36] Ibid. [37] Richard Côté, EACL, Témoignages, 19 octobre 2009. [38] Robert Atcher, International SNM, Témoignages, 21 août 2009. [39] Serge Dupont, Ressources naturelles Canada, Témoignages, 2 juin 2009. [40] Jean Koclas, École polytechnique Montréal, Témoignages, 18 juin 2009. [41] Phillippe Hébert, Covidien, Témoignages, 30 mars 2010, et Cyrille Villeneuve, Lantheus Imagerie Médicale, Témoignages, 25 mars 2010. [42] Jean-Luc Urbain, Association canadienne de médecine nucléaire, Témoignages, 19 octobre 2009. [43] Kevin Tracey, Association ontarienne de médecine nucléaire, Témoignages, 19 octobre 2009. [44] Dominic Ryan, Institut canadien de la diffusion des neutrons, Témoignages, 16 juin 2009. [45] Ibid. [46] Christopher Heysel, Université McMaster, Témoignages, 16 juin 2009. [47] Nigel Lockyer, TRIUMF, Témoignages, 16 juin 2009. [48] Dominic Ryan, Institut canadien de la diffusion des neutrons, Témoignages, 16 juin 2009. [49] Daniel Banks, à titre personnel, Témoignages, 25 mars 2010. [50] Ibid. [51] Dominic Ryan, Institut canadien de la diffusion des neutrons, Témoignages, 16 juin 2009. [52] Linda Keen, à titre personnel, Témoignages, 16 juin 2009. [53] Rapport du Groupe d'experts sur la production d'isotopes médicaux, 30 novembre 2009, http://www.rncan.gc.ca/eneene/sources/uranuc/pdf/panrep-rapexp-fra.pdf. [54] Groupe interservices ad hoc de la Commission européenne concernant l'approvisionnement en radio-isotopes à usage médical, Preliminary Report on Supply of Radioisotopes for Medical Use and Current Development in Nuclear Medicine, 30 octobre 2009. [55] Meena Ballantyne, Direction générale des produits de santé et des aliments, Santé Canada, Témoignages, 2 juin 2009. [56] Ibid. [57] Karen Gulenchyn, département de médecine nucléaire, Hamilton Health Sciences et St. Joseph's Healthcare Hamilton, Témoignages, 9 juin 2009. [58] Éric Turcotte, Centre d'imagerie moléculaire de Sherbrooke, à titre personnel, Témoignages, 25 mars 2010. [59] Groupe interservices ad hoc de la Commission européenne concernant l'approvisionnement en radio-isotopes à usage médical, Preliminary Report on Supply of Radioisotopes for Medical Use and Current Development in Nuclear Medicine, 30 octobre 2009. [60] Cyrille Villeneuve, Lantheus Imagerie Médicale, Témoignages, 25 mars 2010. [61] Éric Turcotte, Centre d'imagerie moléculaire de Sherbrooke, à titre personnel, Témoignages, 25 mars 2010. [62] Ibid. [63] Nigel Lockyer, TRIUMF, Témoignages, 16 juin 2009. [64] Éric Turcotte, Centre d'imagerie moléculaire de Sherbrooke, à titre personnel, Témoignages, 25 mars 2010. [65] Jean-Luc Urbain, Association canadienne de médecine nucléaire, Témoignages, 19 octobre 2009. [66] Éric Turcotte, Centre d'imagerie moléculaire de Sherbrooke, à titre personnel, Témoignages, 25 mars 2010. [67] Meena Ballantyne, Direction générale des produits de santé et des aliments, Santé Canada, Témoignages, 2 juin 2009. [68] Karen Gulenchyn, département de médecine nucléaire, Hamilton Health Sciences et St. Joseph's Healthcare Hamilton, Témoignages, 9 juin 2009. [69] Tim Meyer, TRIUMF, Témoignages, 25 mars 2010. [70] Cyrille Villeneuve, Lantheus Imagerie Médicale, Témoignages, 25 mars 2010. [71] Tim Meyer, TRIUMF, Témoignages, 25 mars 2010. [72] Jean-Luc Urbain, Association canadienne de médecine nucléaire, Témoignages, 19 octobre 2009. [73] Rapport du Groupe d'experts sur la production d'isotopes médicaux, 30 novembre 2009, http://www.rncan.gc.ca/eneene/sources/uranuc/pdf/panrep-rapexp-fra.pdf. [74] Ibid. [75] Ibid. [76] Serge Dupont, Ressources naturelles Canada, Témoignages, 2 juin 2009. [77] Hugh MacDiarmid, EACL, Témoignages, 4 juin 2009. [78] Ibid., 21 août 2009. [79] Jean Koclas, École polytechnique Montréal, Daniel Meneley, University of Ontario Institute of Technology, et Jatin Nathwani, Université de Waterloo, Témoignages, 18 juin 2009. [80] Steve West, MDS Nordion, Témoignages, 11 juin 2009. [81] John Waddington, conseiller en sûreté nucléaire, Témoignages, 11 juin 2009. [82] Hugh MacDiarmid, EACL, Témoignages, 4 juin 2009. [83] Rapport du Groupe d'experts sur la production d'isotopes médicaux, 20 novembre 2009, http://www.rncan.gc.ca/eneene/sources/uranuc/pdf/panrep-rapexp-fra.pdf. [84] Daniel Banks, à titre personnel, Témoignages, 25 mars 2010. [85] Christopher Heysel, directeur, Activités et installations nucléaires, McMaster Nuclear Reactor, Université McMaster, Témoignages, 16 juin 2009. [86] Ibid. [87] Hugh MacDiarmid, EACL, Témoignages, 21 août 2009. [88] Rapport du Groupe d'experts sur la production d'isotopes médicaux, 30 novembre 2009, http://www.rncan.gc.ca/eneene/sources/uranuc/pdf/panrep-rapexp-fra.pdf. [89] Université McMaster, Nuclear Engineering and Science, http://engphys.mcmaster.ca/research/areas/nuc.htm. [90] Tim Meyer, TRIUMF, Témoignages, 25 mars 2010. [91] Rapport du Groupe d'experts sur la production d'isotopes médicaux, 30 novembre 2009, http://www.rncan.gc.ca/eneene/sources/uranuc/pdf/panrep-rapexp-fra.pdf. [92] Ibid. [93] Ibid. [94] Ibid. [95] Tim Meyer, TRIUMF, Témoignages, 25 mars 2010. [96] Rapport du Groupe d'experts sur la production d'isotopes médicaux, 30 novembre 2009, http://www.rncan.gc.ca/eneene/sources/uranuc/pdf/panrep-rapexp-fra.pdf. [97] Nigel Lockyer, TRIUMF, Témoignages, 16 juin 2009. [98] Rapport du Groupe d'experts sur la production d'isotopes médicaux, 30 novembre 2009, http://www.rncan.gc.ca/eneene/sources/uranuc/pdf/panrep-rapexp-fra.pdf. [99] Ibid. [100] Serge Dupont, Ressources naturelles Canada, Témoignages, 21 août 2009. [101] Richard Côté, EACL, Témoignages, 19 octobre 2009. [102] Steve West, MDS Nordion, Témoignages, 11 juin 2009. [103] Serge Dupont, Ressources naturelles Canada, Témoignages, 2 juin 2009. [104] Réponse du gouvernement du Canada au rapport du Groupe d'experts sur la production d'isotopes médicaux, 31 mars 2010. [105] Budget de 2010, http://www.budget.gc.ca/2010/pdf/budget-planbudgetaire-fra.pdf. [106] Réponse du gouvernement du Canada au rapport du Groupe d'experts sur la production d'isotopes médicaux, 31 mars 2010. [107] Selon EACL, la majeure partie des fonds sont réservés « aux besoins financiers imprévus associés au parachèvement des projets visant à prolonger la durée de vie utile des centrales de Bruce Power et de Point Lepreau ». Voir Hugh MacDiarmid, EACL, Témoignages, 30 mars 2010. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||